Khảo sát miễn dịch trong nghiên cứu phát triển vaccine SARS-CoV-2
Đăng bởi Ngâu Nguyễn - - 03/19/2021Tác giả: Chelsea Pratt và Leala Thomas – Bio-Rad Laboratories
Khả năng phát hiện chuyên biệt từng mục tiêu của đáp ứng miễn dịch qua trung gian tế bào là rất quan trọng trong quá trình phát triển vắc xin. Hãy cùng khám phá cách hệ thống phân tích tế bào ZE5 được sử dụng để phát hiện các marker hoạt hóa miễn dịch, định lượng cytokine nội bào và xác định các kháng thể đặc hiệu với protein một cách nhanh chóng, với hiệu suất cao.
Vaccine được tạo ra như thế nào?
Để phát triển một loại vaccine an toàn và hiệu quả, cần phải có kiến thức về cấu trúc mầm bệnh, cơ chế xâm nhập và cách thức lây nhiễm và lây lan của mầm bệnh trên khắp cơ thể. Kiến thức này góp phần vào việc lựa chọn kháng nguyên vaccine bằng cách cung cấp thông tin cơ sở về cách hệ thống miễn dịch của cơ thể phản ứng trong quá trình nhiễm trùng.
Ứng cử viên kháng nguyên dùng làm vaccine tối ưu sẽ bắt chước một trong những thuộc tính này, giúp hệ thống miễn dịch được diễn tập trước việc tiếp xúc với tác nhân lây nhiễm. Quá trình này dẫn đến tạo ra các kháng thể trung hòa các kháng nguyên đó. Trong quá trình xây dựng vaccine, các kháng nguyên đã chọn sẽ được theo dõi về độ ổn định, độ an toàn và độ hiệu quả, bao gồm cả tính sinh miễn dịch, trong các thử nghiệm tiền lâm sàng và lâm sàng. (Cunningham et al. 2016).
Tầm quan trọng của protein gai (Spike protein) của SARS-CoV-2
Điều vô cùng quan trọng trong quá trình phát triển vaccine là tìm ra mục tiêu của phản ứng miễn dịch qua trung gian tế bào. Trong đại dịch COVID-19, các nhà khoa học tại Đại học Washington (Seattle, Hoa Kỳ) và Humabs BioMed SA (Thụy Sĩ) đã hợp tác nghiên cứu cơ chế gây bệnh của SARS-CoV-2 ở người.
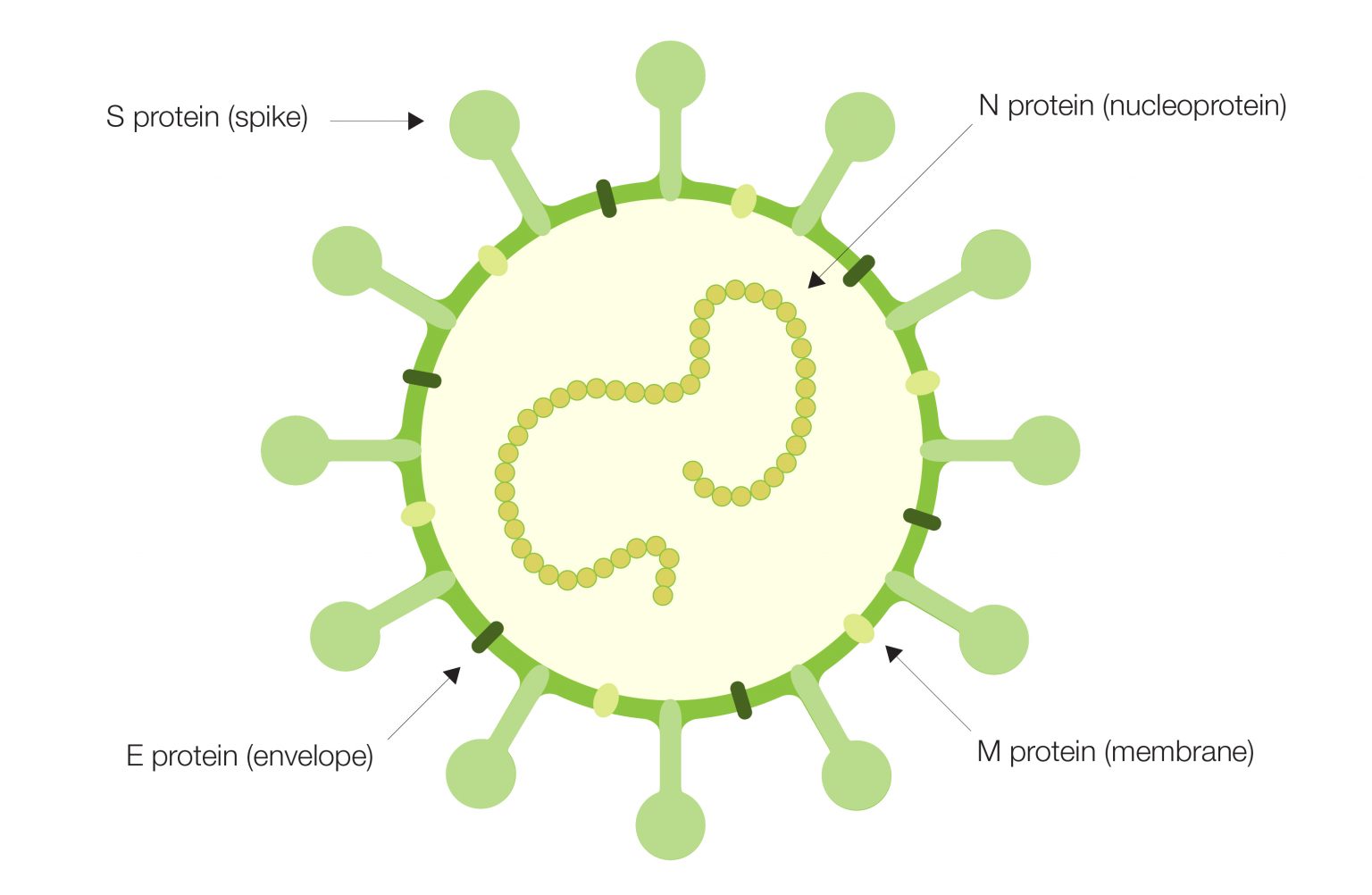
Nhóm nghiên cứu đã xác định các kháng thể trung hòa từ bệnh nhân nhiễm COVID-19 đang điều trị, và nhất quán rằng ~ 90% kháng thể có liên kết với vùng receptor-binding domain (RBD) của protein gai (spike (S) protein) trên bề mặt của virus. Phát hiện này cho thấy tầm quan trọng của S-protein đối với sự lây truyền virus và sự tiến triển của bệnh. Một kháng thể trung hòa đặc biệt đã khóa RBD trong một cấu trúc mở, cung cấp thêm thông tin về cấu trúc cho việc thiết kế kháng nguyên vaccine (Pinto và cộng sự 2020).
Điều thú vị là các nhà khoa học đã lưu ý thêm rằng sự tiến triển của bệnh COVID-19 khác nhau giữa các bệnh nhân, chủ yếu dựa trên độ tuổi. Bệnh nhân nhỏ tuổi, trẻ em và thanh thiếu niên hiếm khi phát triển các triệu chứng đáng kể và thậm chí ít phát triển các biến chứng từ các triệu chứng này. Để kiểm tra khả năng miễn dịch dịch thể, hai nghiên cứu riêng biệt đã kiểm tra huyết thanh của những bệnh nhân chưa bị nhiễm SARS-CoV-2 trước đó, cũng như các mẫu huyết thanh được thu thập trước khi đại dịch bùng phát.
Trong cả hai nghiên cứu, các kháng thể phản ứng chéo (cross-reactive antibodies) có tương tác đặc hiệu với protein S đã được phát hiện và đó là lý do đằng sau sự không đồng nhất được quan sát thấy trong các bước tiến triển của bệnh (Mateus et al. 2020, Ng et al. 2020). Những dữ liệu này nhắc lại tầm quan trọng của protein S trong cả hai quá trình truyền tải virus lẫn phản ứng miễn dịch.
Phương pháp đếm tế bào theo dòng chảy (Flow cytometry) hỗ trợ nghiên cứu miễn dịch học nhanh chóng
Trong tất cả các nghiên cứu được đề cập ở trên, hệ thống phân tích tế bào Bio‑Rad ZE5 được sử dụng để phát hiện các marker cảm ứng miễn dịch, định lượng các cytokine nội bào hoặc xác định các kháng thể đặc hiệu với protein S một cách nhanh chóng, với hiệu suất cao.
Trên thực tế, Viện Francis Crick (Anh) đã thiết lập một quy trình xét nghiệm huyết thanh học tối ưu sử dụng máy phân tích tế bào ZE5 để hỗ trợ sàng lọc nhanh các kháng thể trong huyết thanh có phản ứng với kháng nguyên SARS-CoV-2 (Russell và cộng sự 2020). Trong nghiên cứu đó, các tế bào HEK293T biểu hiện tiểu đơn vị S-protein của SARS-CoV-2 được ủ với huyết thanh của người tham gia và nhuộm bằng kháng thể kháng IgG, IgM và IgA liên hợp huỳnh quang trước khi thực hiện sàng lọc với hiệu suất cao trên máy phân tích tế bào ZE5.
Một nghiên cứu bổ sung được thực hiện để tìm hiểu tỷ lệ nhiễm bệnh tiềm ẩn của nhân viên y tế tuyến đầu ở London, máy phân tích tế bào ZE5 đã được sử dụng cùng với xét nghiệm RT-PCR cho SARS-CoV-2 như một phần của quy trình xét nghiệm huyết thanh học triệt để (Houlihan và cộng sự 2020). Điều này cho thấy tính linh hoạt và tốc độ của công nghệ đo tế bào theo dòng chảy cùng với các tính năng tự động hóa, trong việc giải quyết những thách thức chính khi cần khảo sát thông tin miễn dịch.
Tầm quan trọng của miễn dịch học
Sự phát triển nhanh chóng của vaccine COVID-19 không thể đạt được nếu không có kiến thức về vai trò của protein S trong quá trình sinh bệnh của coronavirus. Điều quan trọng không kém là xác định vai trò của các miền phụ của protein trong việc vô hiệu hóa loại virus mới này, vì vậy cần có các nghiên cứu thăm dò và phân tích phản ứng miễn dịch của bệnh nhân đối với virus
Trong khi các công nghệ vaccine axit nucleic đã phát triển để có thể đáp ứng với tốc độ phát triển nhanh chóng của vaccine trong đại dịch, chúng sẽ không hiệu quả nếu các nhà nghiên cứu không thể nhanh chóng xác định kháng nguyên tốt nhất và hiệu quả nhất - RBD của protein S.
Để biết thêm về các công cụ phát triển vaccine từ Bio-Rad, hãy xem trang Giải pháp Miễn dịch học cho Nghiên cứu Coronavirus của chúng tôi.
Tài liệu tham khảo
Cunningham AL et al. (2016). Vaccine development: From concept to early clinical testing. Vaccine 34, 6,655–6,664.
Houlihan CF et al. (2020). Pandemic peak SARS-CoV-2 infection and seroconversion rates in London frontline health-care workers. Lancet 396, e6–e7.
Mateus J et al. (2020). Selective and cross-reactive SARS-CoV-2 T cell epitopes in unexposed humans. Science 370, 89–94.
Ng KW et al. (2020). Preexisting and de novo humoral immunity to SARS-CoV-2 in humans. Science 370, 1,339–1,343.
Pinto D et al. (2020). Cross-neutralization of SARS-CoV-2 by a human monoclonal SARS-CoV2 antibody. Nature 583, 290–295.
Russell E et al. (2020). Adapting to the coronavirus pandemic: Building and incorporating a diagnostic pipeline in a shared resource laboratory. Cytometry 99, 90–99.
Những bản tin khác: |